Россия
Москва, г. Москва и Московская область, Россия
АНО ДПО "Московский медико-социальный институт имени Ф.П. Гааза", Москва (Кафедра профилактической медицины, Заведующий)
АНО ДПО "Московский медико-социальный институт имени Ф.П. Гааза", Москва (Кафедра внутренних болезней, профессор)
Москва, г. Москва и Московская область, Россия
Россия
ВАК 14.01.2017 Хирургия
ВАК 14.01.1931 Пластическая хирургия
УДК 61 Медицина. Охрана здоровья
ГРНТИ 76.29 Клиническая медицина
ОКСО 31.06.2001 Клиническая медицина
ОКСО 31.07.01 Клиническая медицина
ББК 53 Клиническая медицина в целом
ТБК 573 Клиническая медицина в целом
BISAC MED085020 Surgery / Oral & Maxillofacial
Актуальность. Современная техника позволяет не только виртуально планировать реконструктивную операцию, но, также, по результатам планирования, изготавливать шаблоны для выполнения резекции и остеотомии, а также индивидуальные реконструктивные пластины из титана. Целью данной статьи являлся анализ результатов применения аддитивных технологий для планирования и выполнения реконструктивных операций в Центре челюстно-лицевой хирургии и стоматологии ФГБУ «ГВКГ им. Н.Н.Бурденко». Материалы и методы. В период с 2007 года по 2017 год в центре челюстно-лицевой хирургии и стоматологии было выполнено 144 операции по устранению дефектов костей раз-личной локализации. В большинстве случаев - 93% (136 пациентов) отмечались дефекты костей лицевого скелета и свода черепа. В двух случаях требовалось устранить дефект ключицы, в одном случае - дефект ладьевидной кости, в одном случае дефект лучевой кости, в двух случаях - дефект плечевой кости, в двух случаях - дефект бедренной кости. Результаты. Для устранения дефектов в 87% случаев (125 пациентов) использовали реваскуляризированные аутотрансплантаты, в 13% случаев (19 пациентов) - аллопластические материалы. Аддитивные технологии использовали в 85% (n=123) случаев для планирования операции по устранению дефектов, а также для изготовления хирургических моделей и шаблонов. Приведены клинические случаи в качестве примеров использования аддитивных технологий для планирования реконструктивных операций по устранения костных дефектов различной локализации. Частота послеоперационных осложнений в группе пациентов с дефектами костей лицевого скелета и свода черепа, которым проводили оперативные вмешательства с использованием шаблонов, составила 26%, в том числе малых осложнений – 17,5%, больших – 8,5%. Среди малых осложнений преобладали гематомы (5%) и нагноения (5%) реципиентной раны, реже аналогичные осложнения – гематомы (4%) и нагноения (3%) донорской раны. Большие осложнения были представлены случаями полного (4%) или частичного (5%) некроза трансплантата. При оперативных вмешательствах без шаблона потребовалось достоверно больше среднего времени забора и формирования трансплантата (212 ± 18,7 мин), чем при операциях с шаблоном, в том числе с направителем для сверления (136 ± 12,6 мин, p <0,001) и без направителя для сверления (160 ± 16,3 мин, p <0,001). Заключение. Применение в ходе реконструктивных операций хирургических моделей и шаблонов сокращает время самой операции и уменьшает число послеоперационных осложнений.
аддитивные технологии, виртуальное хирургическое планирование, прототипирование, ре-конструктивная хирургия, челюстно-лицевая хирургия, нижняя челюсть, малоберцовый трансплантат, послеоперационные осложнения
Список сокращений
ВХП – виртуальное хирургическое планирование
КЛКТ – конусно-лучевая компьютерная томография
МСКТ – мульти-спиральная компьютерная томография
УЗДС – ультразвуковое дуплексное сканирование
ИПЛИТ РАН- Институт проблем информационных и лазерных технологий Российской академии наук
ЛСОИ - лаборатории средств отображения информации
СОПР – слизистая оболочка полости рта
Введение
Основная цель реконструктивной хирургии челюстно-лицевой области заключается в максимальном восстановлении функции и внешности пациента. Высокотехнологичные методы реконструктивной хирургии могут быть предпочтительнее, чем традиционные, если в большей степени отвечают этим требованиям [1]. Виртуальное моделирование операции на челюстно-лицевой области в значительной степени сокращает время операции и увеличивает точность ее исполнения [2,3]. Современная техника позволяет не только планировать реконструктивную операцию виртуально, но также, по результатам планирования, получать шаблоны для выполнения резекции и остеотомии, а также индивидуальные реконструктивные пластины из титана [4]. Применение новых методов приводит к снижению частоты осложнений и улучшению результатов хирургического лечения [3], является частью обучения и повышения квалификации врачей [5].
Аддитивные технологии - процесс создания физического объекта на основе цифровых данных трехмерной компьютерной модели путем послойного добавления материала [6]. Применяющийся ранее для описания этого процесса термин «быстрое прототипирование» (Rapid Prototyping) было рекомендовано изъять из обращения как утративший смысл для современных аддитивных технологий. Это связано с тем, что изготовление моделей и макетов на 3D-принтерах превратилось в создание конечных и серийных продуктов, применительно к которым использовать термин «прототип» нельзя. Особенно быстро эти технологии развиваются в точном машиностроении, аэрокосмической отрасли, военно-промышленном комплексе США и Западной Европы. Данные технологии нашли свое применение и в медицине практически сразу после создания первого 3D-принтера. Основные области применения аддитивных технологий в медицине - реконструктивная хирургия и протезирование [7,8].
Аддитивные технологии предполагают наличие двух ключевых звеньев: программного обеспечения, позволяющего создавать трехмерные компьютерные модели, и 3D принтера, способного создавать физический объект на основе его цифровой модели. Программное обеспечение для создания трехмерных компьютерных моделей может быть универсальным, либо рассчитано для решения специальных задач. Например, программа Simplant (производитель Materialise, Бельгия) предназначена для планирования операции дентальной имплантации и создания компьютерных моделей хирургических шаблонов для ее выполнения. Другая программа - ProPlan той же фирмы, предназначена для планирования реконструктивной операции на нижней челюсти с применением малоберцового реваскулиризированного трансплантата, создания компьютерных моделей хирургических шаблонов и реконструктивной пластины для получения запланированного результата в операционной. Для работы в этих программах информация о пациенте загружается в виде данных компьютерной томографии (конусно-лучевой (КЛКТ) либо мультиспиральной (МСКТ)). Эти программы дороги, рассчитаны на использование в работе инструментов и расходных материалов определенного производителя. Так, в случае последней программы, это инструменты и расходные материалы фирмы Synthes (Швейцария). Все это делает данные продукты практически недоступными пациентам большинства стран, включая такие страны Старого Света, как Италия, Испания и др., где расходы на медицину меньше, чем в таких странах, как Германия, Австрия, Швейцария. Существуют и другие программные решения, позволяющие создавать трехмерные компьютерные модели с нуля. Примером могут служить программы Mimics и Magics (производитель Materialise, Бельгия). Их мощный функционал также включает возможность построения трехмерных компьютерных моделей биологических объектов по данным компьютерной томографии. Однако, работа с ними требует специальной подготовки и значительной затраты времени.
Созданные в упомянутых выше программах трехмерные модели печатают на трехмерных принтерах. Для печати физической модели могут быть использованы различные материалы. Выбор материала зависит от предназначения печатаемого объекта. Так, хирургические модели и шаблоны могут быть созданы из пластика или гипса (рис. 1). При печати изделий, предназначенных для имплантации в организм человека, используется, как правило, титан (рис. 2).

Рис. 1. Печать пластиковых моделей и шаблонов на отечественном 3D принтере ЛС-250 в ИПЛИТ РАН (г. Шатура)
Fig. 1. Printing plastic models and templates on the domestic 3D printer LS-250

Рис. 2. Печать имплантатов из титана на 3D принтере в «Эндопринт» (г.Москва)
Fig. 2. Printing of titanium implants on a 3D printer in the "Endprint" (Moscow)
Целями данной работы являлись: анализ результатов применения аддитивных технологий для планирования и выполнения реконструктивных операций в Центре челюстно-лицевой хирургии и стоматологии ФГБУ «ГВКГ им. Н.Н. Бурденко»; оценка эффективности использования шаблонов при реконструктивных оперативных вмешательствах при дефектах костей лицевого скелета и свода черепа, и влияния использования шаблонов на послеоперационные осложнения.
Материалы и методы
В период с 2007 г. по 2017 г. в нашем Центре было выполнено 144 операции по устранению дефектов костей различной локализации с компьютерным планированием. Для осуществления компьютерного планирования реконструктивных операций мы используем материальную базу Института проблем информационных и лазерных технологий Российской академии наук (ИПЛИТ РАН) (г. Шатура, Московская область) с 2004 года. Научные сотрудники лаборатории средств отображения информации (ЛСОИ) ИПЛИТ РАН имеют богатый опыт работы с программами Mimics и Magics (производитель Materialise, Бельгия). Для осуществления планирования мы выполняли МСКТ области, в которой должна была проводиться операция. Пакет полученных данных отправляли электронной почтой в ИПЛИТ РАН. После подготовки трехмерных компьютерных моделей объекта операции виртуальное хирургическое планирование выполняли дистанционно с использованием видеоконференцсвязи. При этом хирург фактически осуществлял виртуальную операцию руками инженера ЛСОИ.
Результаты
В большинстве случаев - в 93% (n=136) проведены операции по устранению дефектов костей лицевого скелета и свода черепа (рис. 3). В двух случаях требовалось устранить дефект ключицы, в одном случае - дефект ладьевидной кости, в одном случае дефект лучевой кости, в двух случаях - дефект плечевой кости, в двух случаях - дефект бедренной кости. Возраст пациентов был от 4 лет и 8 месяцев до 79 лет (рис. 4), средний возраст составил 47,5 лет. Этиологией дефектов в основном являлись опухоли 81% (n=117), а также огнестрельные ранения - 10% (n=14), лучевые остеонекрозы - 8% (n=11); дефекты костей в результате травмы возникали в 1% (n=2) случаев (рис. 5). Для устранения дефектов в 87% (n=125) случаев использовали реваскуляризированные аутотрансплантаты, в 13% (n=19) случаев - аллопластические материалы (рис. 6). Аддитивные технологии использовали в 85% (n=123) случаев для планирования операции по устранению дефектов, а также для изготовления хирургических моделей и шаблонов (рис. 7).
Частота послеоперационных осложнений в группе пациентов с дефектами костей лицевого скелета и свода черепа, которым проводили оперативные вмешательства с использованием шаблонов, составила 26%, в том числе малых осложнений – 17,5%, больших – 8,5%. Среди малых осложнений преобладали гематомы (5%) и нагноения (5%) реципиентной раны, реже аналогичные осложнения – гематомы (4%) и нагноения (3%) донорской раны. Большие осложнения были представлены случаями полного (4%) или частичного (5%) некроза трансплантата (рис. 8).
При оперативных вмешательствах без шаблона потребовалось достоверно больше среднего времени забора и формирования трансплантата (212 ± 18,7 мин), чем при операциях с шаблоном, в том числе с направителем для сверления (136 ± 12,6 мин, p <0,001) и без направителя для сверления (160 ± 16,3 мин, p <0,001) (рис. 9).
Далее приведены клинические случаи в качестве примеров использования аддитивных технологий для планирования реконструктивных операций по устранения костных дефектов различной локализации.
Клинический случай 1
Пациентка Б., 28 лет. Деформация свода черепа, скуло-лобно-глазничного комплекса слева после тяжелой черепно-мозговой травмы, резекционной трепанации черепа. Травму получила полгода назад в результате дорожно-транспортного происшествия. Пациентка предъявляла жалобы на двоение в глазах, косметическую неудовлетворенность внешним видом. После обследования было принято решение устранить дефекты и деформации черепно-челюстно-лицевой области имплантатами из титана и хирулена[1], изготовленные по результатам ВХП.
Пациентке была выполнена МСКТ черепа, по результатам которой изготовлена трехмерная компьютерная модель черепа пациентки (рис. 10). Используя такие инструменты программы как Mirroring воссозданы утраченные и деформированные участки черепа (рис. 11). Полученные результаты планирования использованы для печати титановых сетчатых пластин для закрытия дефектов костей свода черепа и создания контурных имплантатов для восстановления дна орбиты и устранения деформации скуло-лобно-глазничного комплекса (рис. 12).
В результате операции положение левого глазного яблока было восстановлено, двоение в глазах исчезло. Контуры лицевого скелета были восстановлены без необходимости выполнять остеотомию, репозицию и остеосинтез смещенных костных фрагментов. При контрольном осмотре через 6 месяцев после операции пациентка была удовлетворена внешним видом. Требовалась незначительная косметическая коррекция рубцов после травмы.
Клинический случай 2
Пациент К., 46 лет. Диагноз: дефект тела и ветви нижней челюсти справа после резекции по поводу рака дна полости рта T2N0M0. Пациент предъявлял жалобы на затруднения при приеме и пережевывании пищи; нарушение речи. Из данных анамнеза и медицинской документации известно, что около года назад пациент был оперирован по поводу рака дна полости рта: выполнена резекция дна полости рта справа, резекция тела и частично ветви нижней челюсти справа. Устранение дефекта не выполнялось. Было принято решение об устранении дефекта нижней челюсти реваскуляризированным трансплантатом из гребня подвздошной кости справа. В плане подготовки к операции была выполнена МСКТ лицевого скелета и тазовых костей. По результатам исследований построены компьютерные модели этих образований. При УЗДС определены реципиентные сосуды на шее (доступны все ветви наружной сонной артерии). УЗДС глубокой артерии, огибающей подвздошную кость, не выполнялось из-за анатомического постоянства сосуда и отсутствия в анамнезе пациента операций в правой подвздошной области. В ходе ВХП обнаружено и исправлено смещение фрагмента правой ветви нижней челюсти (рис. 13). Положение большего фрагмента нижней челюсти также потребовало коррекции и восстановления прикуса из-за его смещения рубцами (рис. 14). После восстановления правильных анатомических взаимоотношений фрагментов нижней челюсти приступили к выбору оптимального донорского места для забора трансплантата. В результате планирования изготовлены хирургические шаблоны-накладки, при помощи которых в операционной были повторены все этапы ВХП (рис. 15). Спустя 10 месяцев после операции пациенту выполнена КЛКТ, которая показала полное приживление трансплантата и практически идеальное восстановление формы нижней челюсти (рис. 16). Зубы верхней и нижней челюсти в ортогнатическом прикусе. Следующий этап лечения планируется установка дентальных имплантатов в трансплантат с последующим протезированием зубов.
Клинический случай 3
Пациентка М., 32 года. Диагноз: несросшийся перелом левой ключицы. Пациентка получила травму за два года до обращения в госпиталь в результате падения с лошади. Было предпринято несколько попыток выполнить репозицию отломков ключицы с остеосинтезом накостной пластиной - без положительного результата. Пациентка предъявляла жалобы на боль в области левой ключицы, ограничение движений левой руки, неудовлетворенность внешним видом из-за наличия деформации в области левой ключицы. При рентгенографии был выявлен перелом пластины, фиксировавшей фрагменты левой ключицы, смещение фрагментов ключицы и ее укорочение (рис. 17). Было принято решение выполнить реконструкцию левой ключицы малоберцовым реваскуляризированным трансплантатом. При ультразвуковом дуплексном сканировании (УЗДС) патологии сосудов голеней и шеи выявлено не было. Для планирования реконструктивной операции выполнена МСКТ ключиц и голеней. Полученные при этом данные использованы для построения трехмерных компьютерных моделей ключиц и малоберцовый костей. В ходе виртуального хирургического планирования (ВХП) использовано зеркальное отражение правой интактной ключицы для позиционирования фрагментов левой ключицы в анатомическом положении (рис. 18). Выполнена резекция измененных краев фрагментов левой ключицы. Подобран участок малоберцовой кости, наилучшим образом восстанавливающий утраченный фрагмент (рис. 19). В завершение ВХП созданы хирургические шаблоны-накладки для точного воспроизведения результата в операционной (рис. 20). После печати пластиковой модели ключицы, восстановленной малоберцовым трансплантатом, и хирургических шаблонов-накладок, по модели ключицы была изогнута и подготовлена к операции реконструктивная титановая пластина для фиксации малоберцового трансплантата в дефекте (рис. 21). Операция выполнялась двумя бригадами хирургов, каждая из которых имела в своем распоряжении необходимые хирургические шаблоны-накладки. Это позволило сократить время операции. Послеоперационный период протекал без особенностей. Швы были сняты амбулаторно. Через год выполнен рентген-контроль результата операции (рис. 22). Форма, контур и длина ключицы полностью восстановлены.
Обсуждение
В большей части случаев (87%) нами применялись реваскуляризированные костные аутотрансплантаты. В течение последних двадцати лет применение реваскуляризированных костных аутотрансплантатов стало золотым стандартом в реконструктивной хирургии нижней челюсти. При этом эффективность этого метода достигает более 90% [9–11]. В работе нами успешно использовались трансплантаты из свободных костно-кожных лоскутов малоберцовой кости.
Использование шаблонов, особенно с направителем для сверления позволило нам достоверно уменьшить среднее время забора и формирования малоберцового трансплантата на 76 минут, что соответствует данным литературы: в исследовании Hanasono M.M. с соавторами (2013) средняя продолжительность операции при использовании шаблонов была на 102 минуты меньше, чем без их использования [2].
Изготовленные стереолитографические модели черепов больных мы использовали также для изгибания реконструктивных титановых пластин с целью фиксации трансплантата, фрагментов челюсти при переломе, что было особенно актуально в случаях с деформацией контура челюсти патологическим процессом и снижало время операции, как и по данным других авторов. В исследовании Prisman E. с соавт. (2014) время, необходимое для изгибания пластины до операции по модели и во время операции, составило в среднем 867 ± 243 секунд и 833 ± 289 секунд соответственно [12].
Использование хирургических шаблонов для формирования трансплантата из свободных костно-кожных лоскутов малоберцовой кости по результатам виртуального планирования устранения дефекта нижней челюсти улучшало результат операции за счет не только снижения времени операции, но и достижения максимального контакта трансплантата и кости.
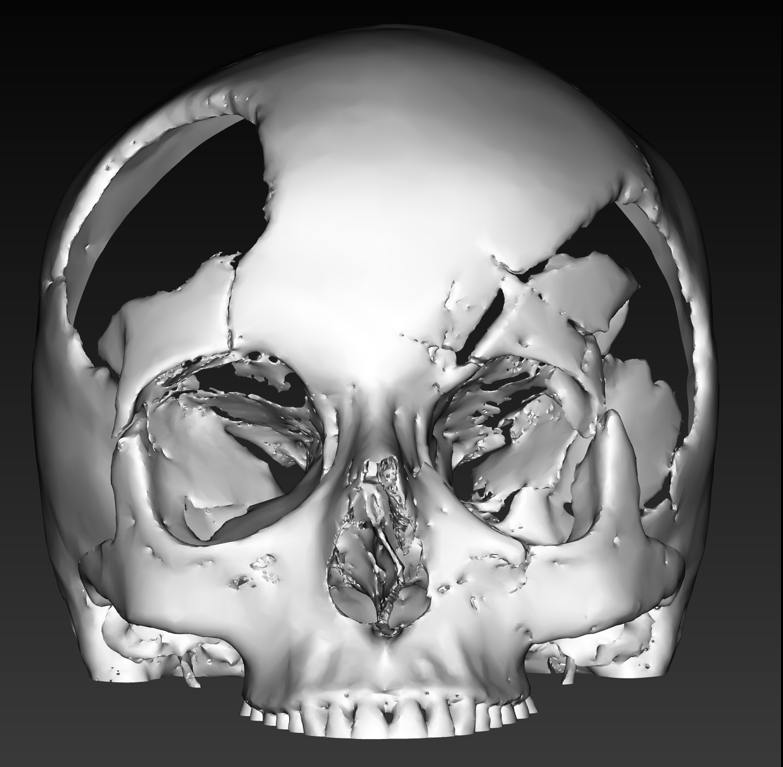
Рис. 10. Трехмерная компьютерная модель черепа пациентки Б.
Fig. 10. 3D computer model of patient B.'s skull
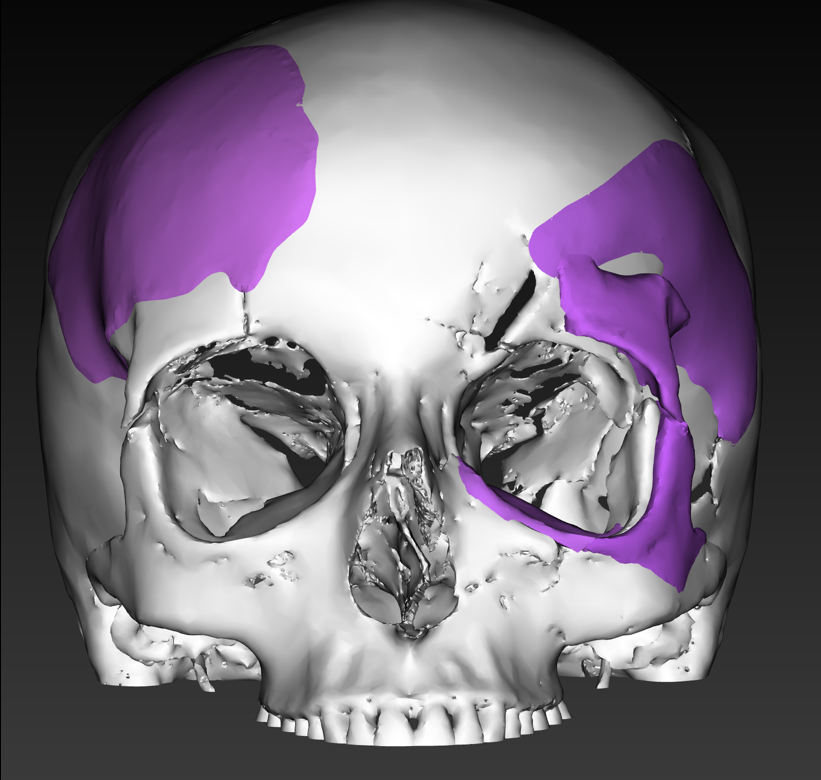
Рис. 11. Трехмерная модель черепа пациентки Б. после устранения дефектов и деформаций в ходе ВХП. Сиреневым цветом отмечены восстановленные участки черепа
Fig. 11. 3D model of patient B.'s skull after elimination of defects and deformities during virtual surgical planning. The restored areas of the skull are marked in lilac
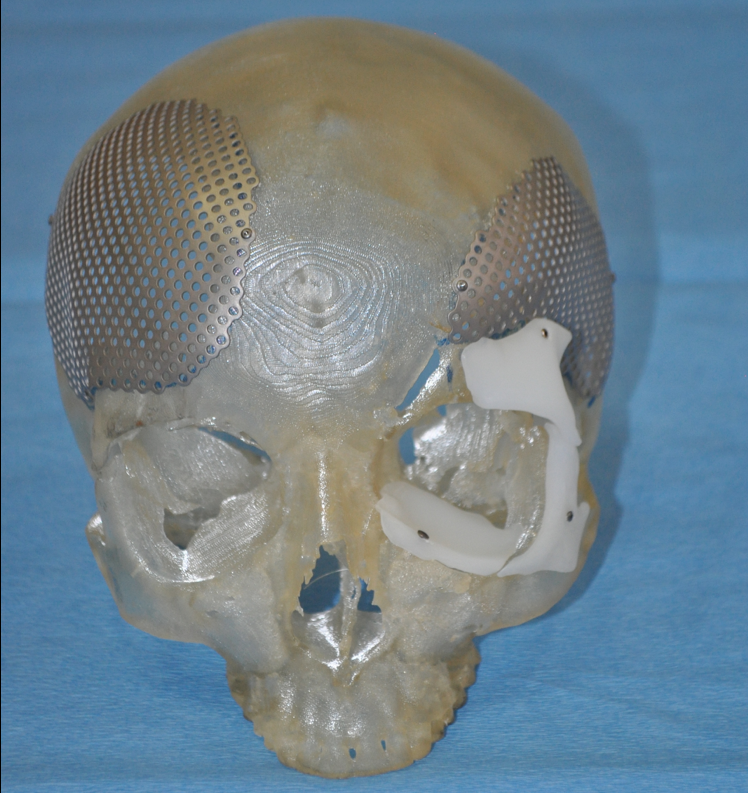
Рис. 12. Физическая модель черепа пациентки Б. с фиксированными имплантатами
Fig. 12. The physical model of the skull of the patient B. with fixed implants
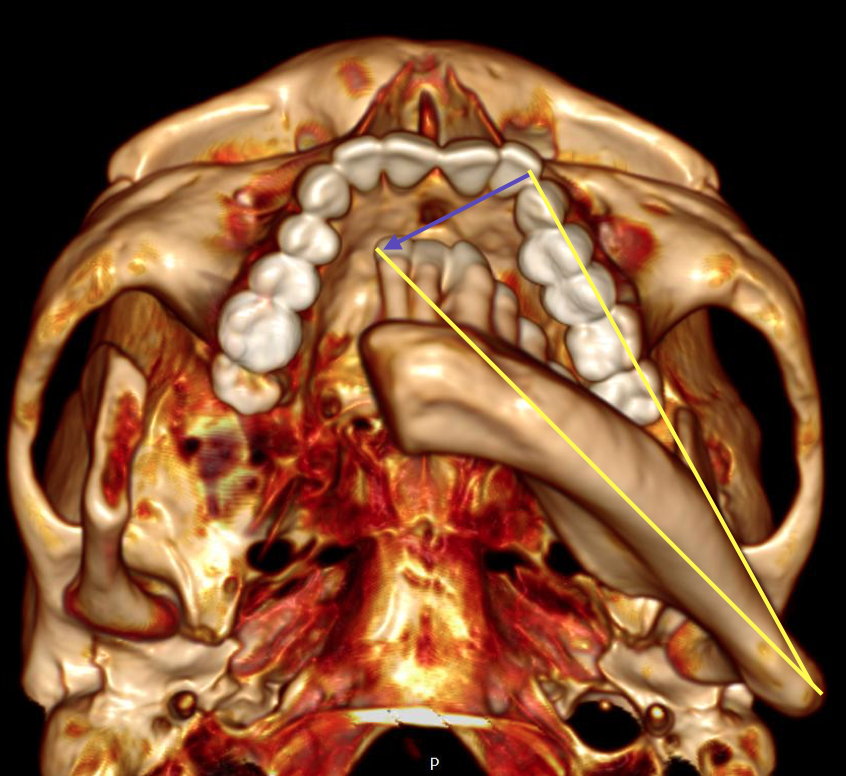
Рис. 13. На трехмерной модели лицевого скелета определяется смещение большего фрагмента нижней челюсти в сторону дефекта (направление указано стрелкой)
Fig. 13. On the 3D model of the facial skeleton, the displacement of a larger fragment of the lower jaw towards the defect is determined (the direction is indicated by an arrow)
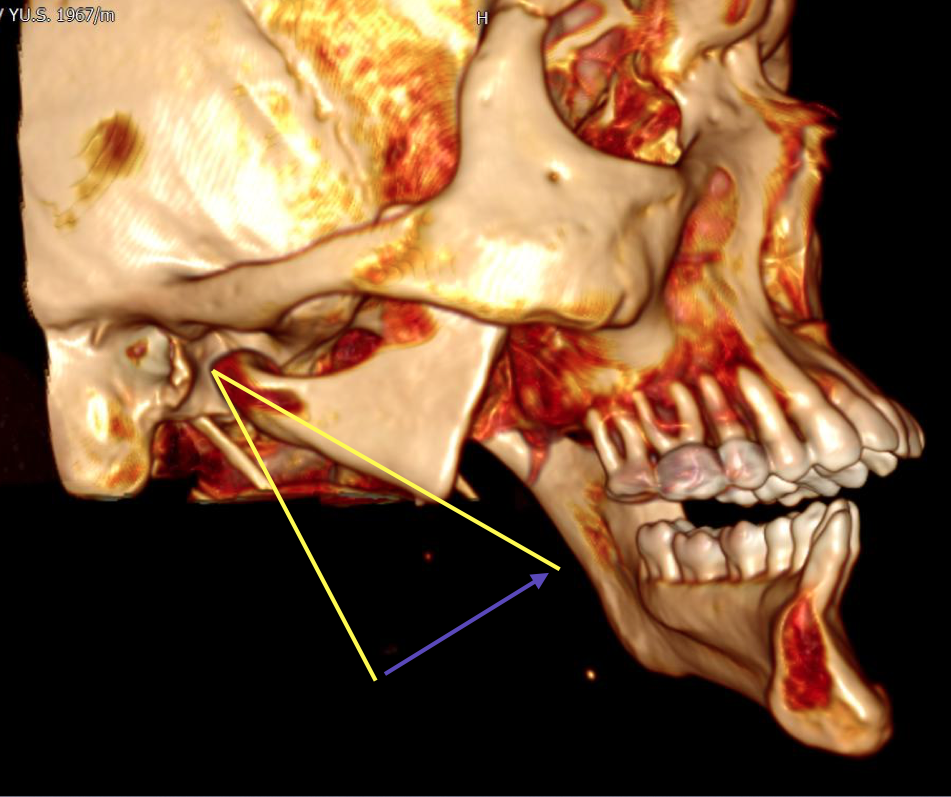
Рис. 14. На трехмерной модели лицевого скелета определяется смещение фрагмента правой ветви нижней челюсти в сторону дефекта (направление указано стрелкой)
Fig. 14. On the 3D model of the facial skeleton, the displacement of the fragment of the right branch of the lower jaw towards the defect is determined (the direction is indicated by an arrow)
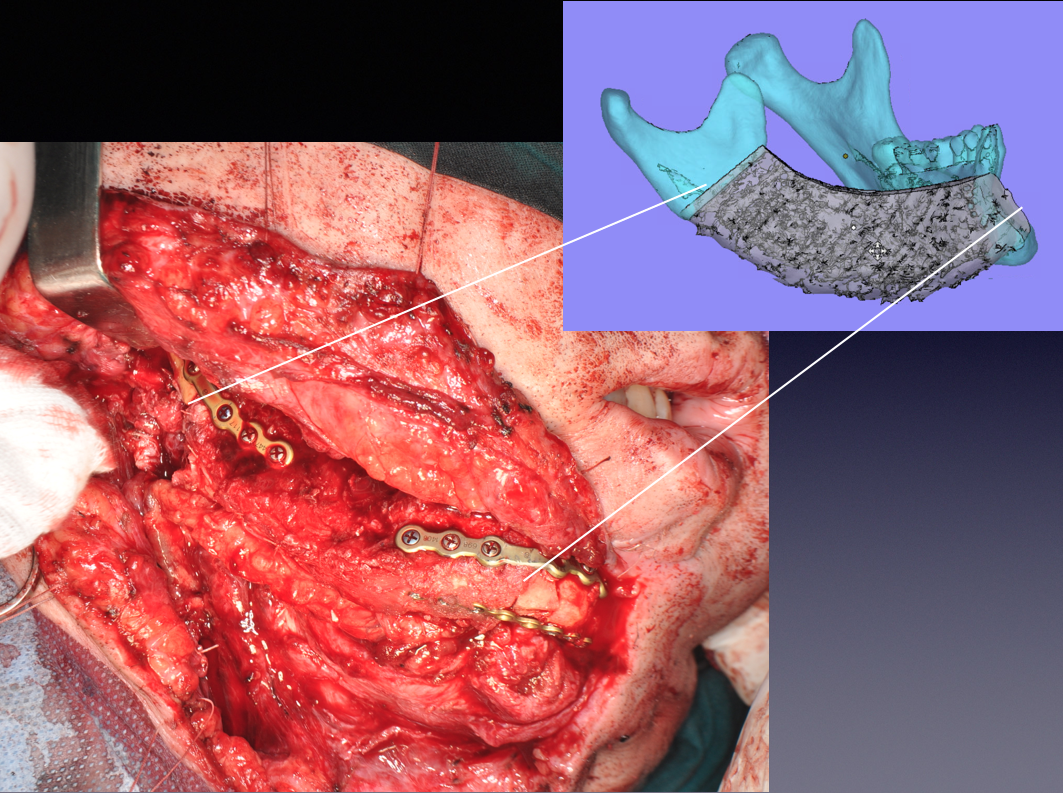
Рис. 15. Трансплантат фиксирован в дефекте нижней челюсти. Его размеры, форма и положение соответствуют компьютерной модели в ходе ВХП
Fig. 15. The graft is fixed in the defect of the lower jaw. Its size, shape and position correspond to the computer model during the virtual surgical planning
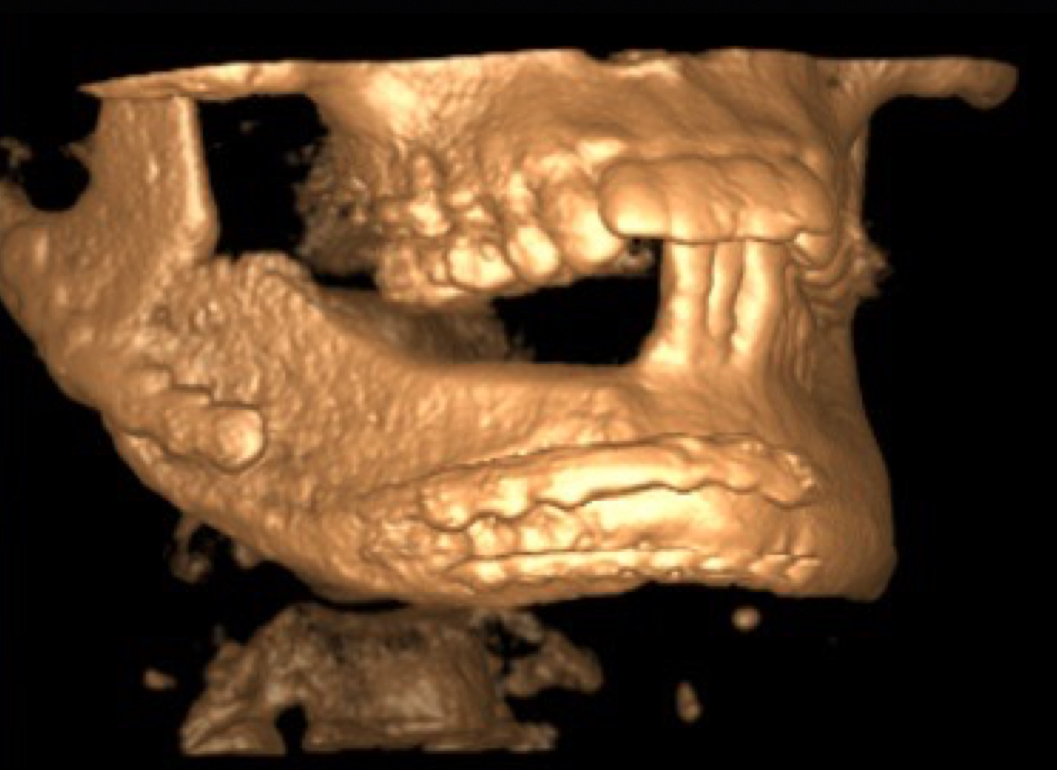
Рис. 16. Трехмерная компьютерная модель нижней челюсти пациента по результатам контрольной КЛКТ
Fig. 16. 3D computer model of the lower jaw of the patient based on the results of cone beam computed tomography (10 months after surgery)
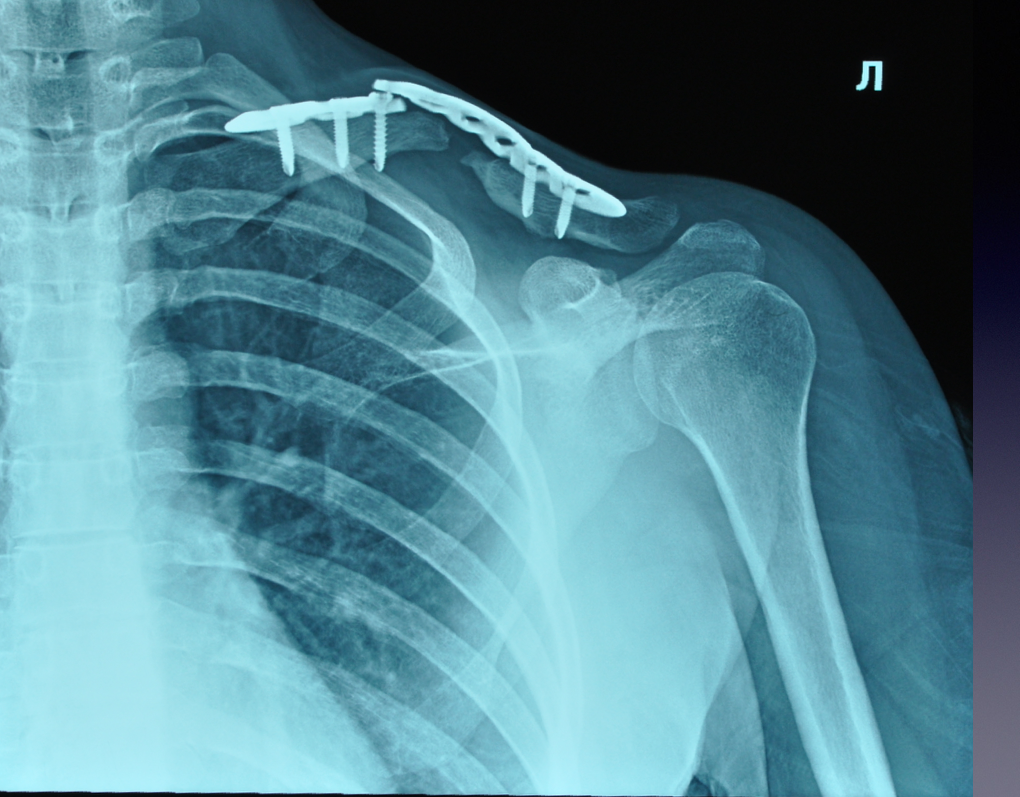
Рис. 17. Рентгенограмма пациентки при поступлении на лечение
Fig. 17. X-ray of the patient at admission to hospital
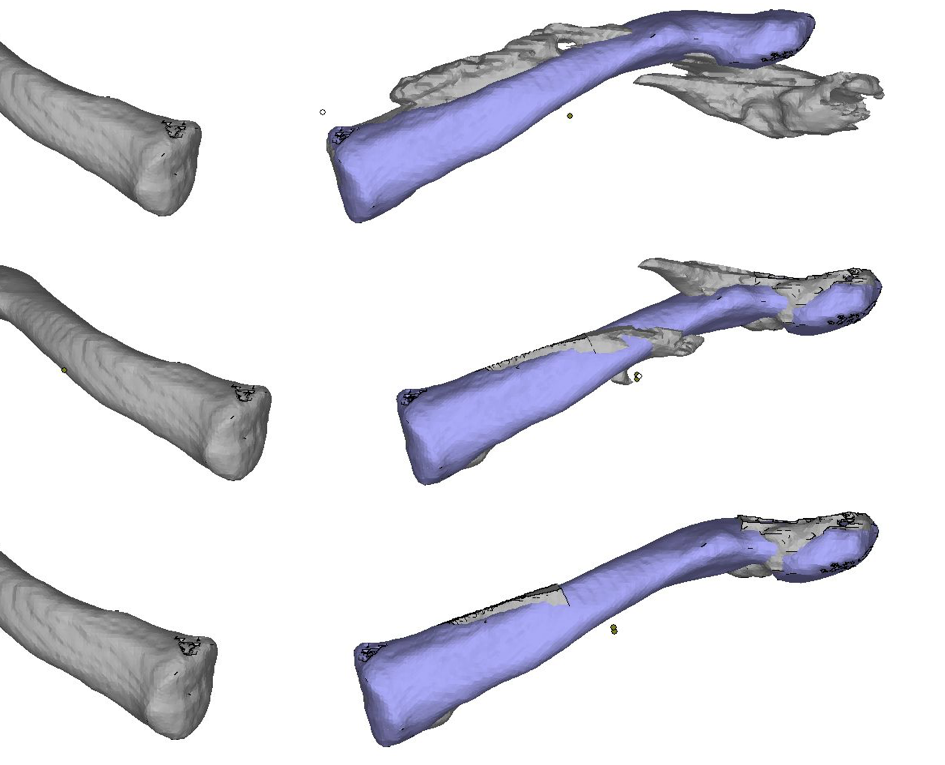
Рис. 18. Первоначальное положение фрагментов ключицы (сверху) и после перемещения их в правильное положение по зеркальному отражению здоровой ключицы
Fig. 18. The initial position of the clavicle fragments (top) and after moving them to the correct position on the mirror image of the healthy clavicle

Рис. 19. Выбор участка малоберцовой кости для устранения дефекта ключицы
Fig. 19. Selection of the fibula area to eliminate the defect of the clavicle
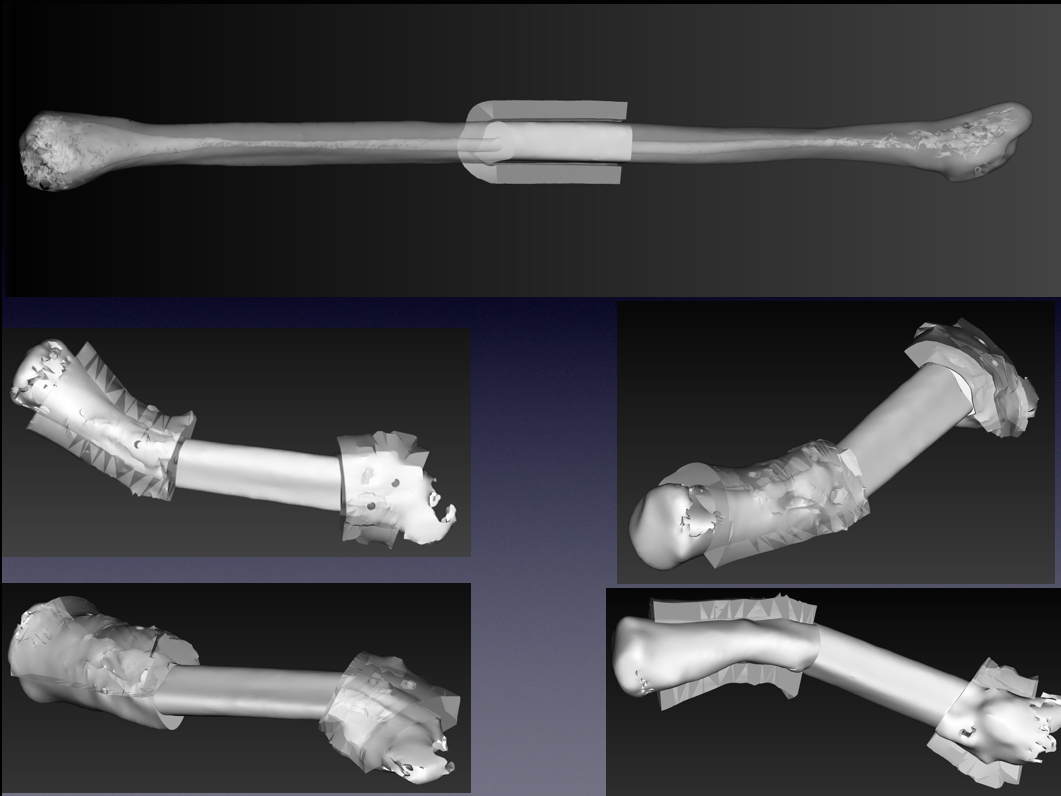
Рис. 20. Компьютерные модели хирургических шаблонов-накладок для выполнения операции
Fig. 20. Computer models of surgical templates-overlays for the operation
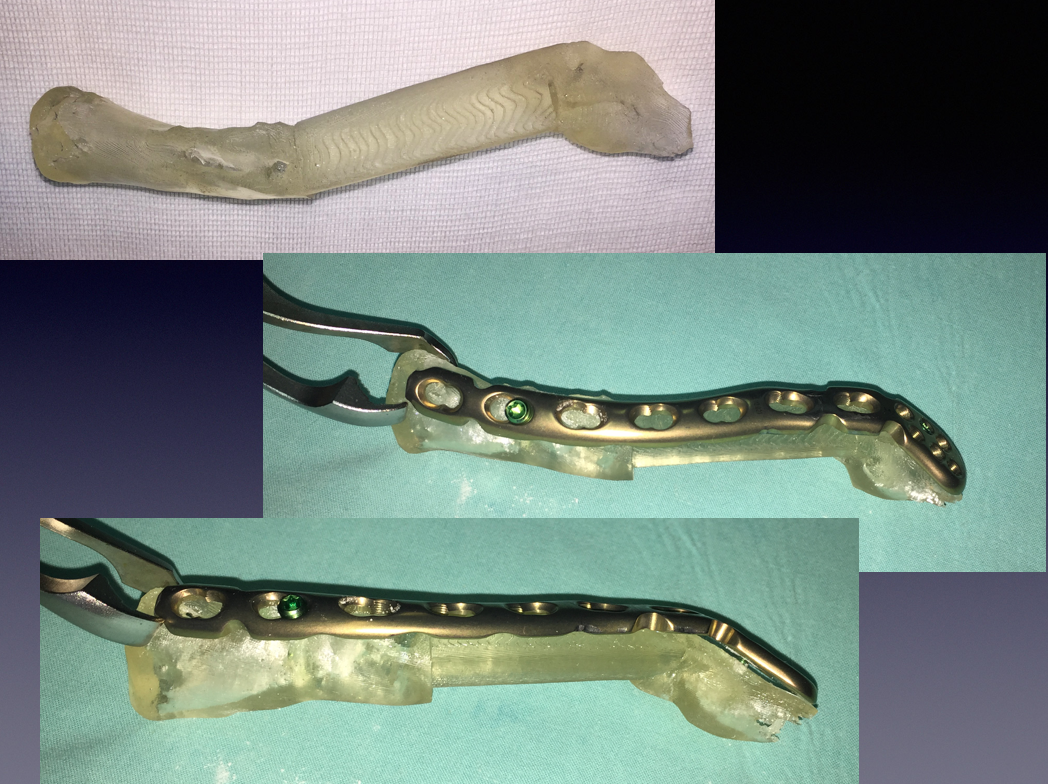
Рис. 21. Подготовка титановой реконструктивной пластины перед операцией
Fig. 21. Preparation of titanium reconstructive plate before surgery
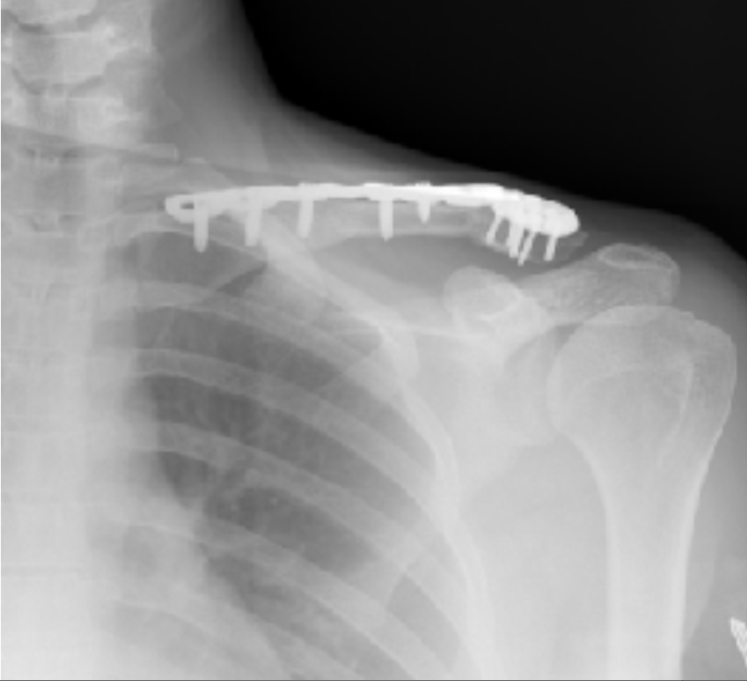
Рис. 22. Рентгенограмма ключицы через один год после операции
Fig. 22. X-ray of the clavicle one year after surgery
Toto J. с соавторами в 2015 оценили результат 8 таких реконструктивных операций. Среднее значение погрешности расстояния между реальными остеотомическими распилами и виртуальными составили 2.06 ± 0.86 mm. Средняя погрешность объема реального трансплантата в сравнении с виртуальным планированием составила 1412.22 ± 439.24 mm3 (9.12% ± 2.84%). А средняя погрешность объема реального трансплантата к его модели составила 2094.35 ± 929.12 mm3 (12.40% ± 5.50%) [3].
Haddock NT с соавт. (2012) показали возможности виртуального хирургического планирования с использованием шаблонов для определения углов распилов трансплантата малоберцовой кости и нижней челюсти для увеличения площади контакта и облегчения хирургического доступа во время операции [13].
Риск больших осложнений (частичного и полного некроза трансплантата) в нашем исследовании был меньше среднего риска по данным литературы. Так, в 2015 году Wong A.K. с соавторами опубликовали результаты анализа факторов риска, оказывающих негативное влияние на выживаемость реваскуляризированных трансплантатов. Ими были изучены материалы более 36 научных статей, а также данные исследования ACS NSQIP (American College of Surgeons National Surgical Quality Improvement Program). Дизайн исследования ACS NSQIP включал в себя 240 переменных, включая предоперационные факторы риска, интраоперационные факторы, а также данные об осложнениях и смертности в течение 30-ти дневного послеоперационного периода. Риск гибели трансплантата у больных, включенных в данное исследование, зависел от локализации дефекта: 9.6% - при локализации в области головы и шеи, 5.6% - в области конечностей, 4.9% - в области молочной железы и 2.5% - в других областях туловища [14].
Заключение
Развитие и совершенствование новых методов реконструктивной хирургии, главным образом реконструктивной микрохирургии, позволяют хирургу устранять дефекты независимо от их этиологии и размеров. Удаление опухоли и устранение дефекта не является критерием выздоровления больного. Восстановление функции утраченного органа полностью или частично и социальная реабилитация пациента - только такой исход может считаться выздоровлением [15]. Использование в работе аддитивных технологий позволило вывести процесс планирования и выполнения реконструктивных операции на новый уровень. Все этапы операции отрабатывались в ходе ВХП до получения желаемого результата. Внутри этой же программной среды создаются хирургические инструменты, которые могут быть напечатаны и применены для выполнения определенной задачи у конкретной пациента. Таким образом, появляется возможность реализации идеи об индивидуальном подходе в лечении больных – персонифицированной медицины.
Применение аддитивных технологий позволяет осуществить трехмерный анализ дефекта или деформации; выбрать оптимальный материал для их устранения; получить представление о результате еще только планируемой операции; создать инструменты для достижения планированного результата операции. Применение в ходе реконструктивных операций хирургических моделей и шаблонов сокращает время самой операции и уменьшает число послеоперационных осложнений. Используемые во время операции хирургические шаблоны, по сути, являются хирургическим инструментом. Их изготовление не требует промышленных мощностей, эти инструменты могут быть напечатаны на 3D-принтере. Такое лечение носит индивидуальный характер, что облегчает реабилитацию пациентов в послеоперационном периоде и повышает качество их жизни.
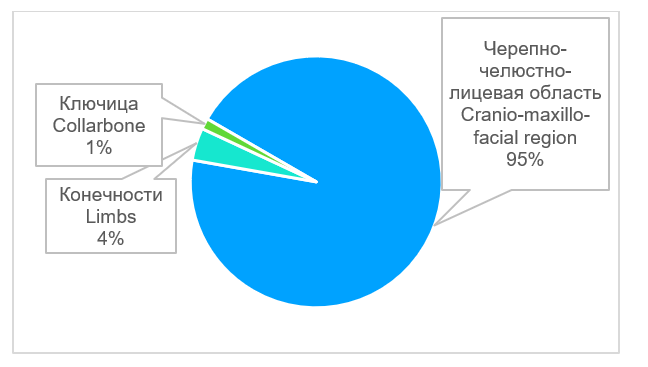
Рис. 3. Область костного дефекта у больных
Fig. 3. Вone defect locations
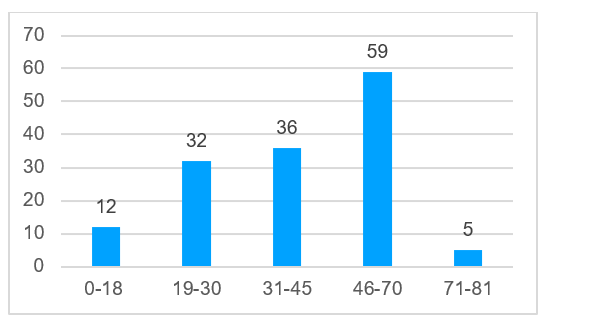
Рис. 4. Возраст пациентов, n = 144
Fig. 4. Patients’ age, n = 144
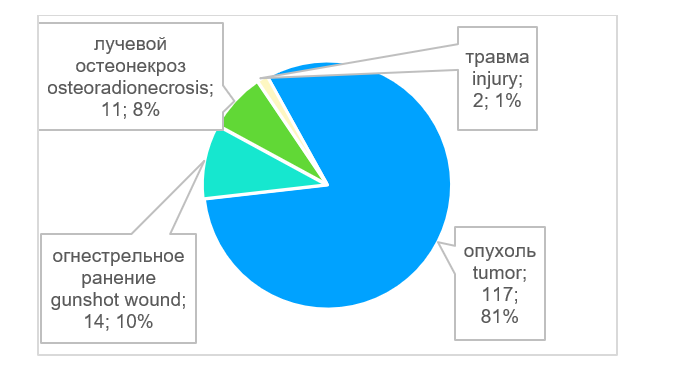
Рис. 5. Этиология костных дефектов, n = 144
Fig. 5. Bone defect etiology, n = 144
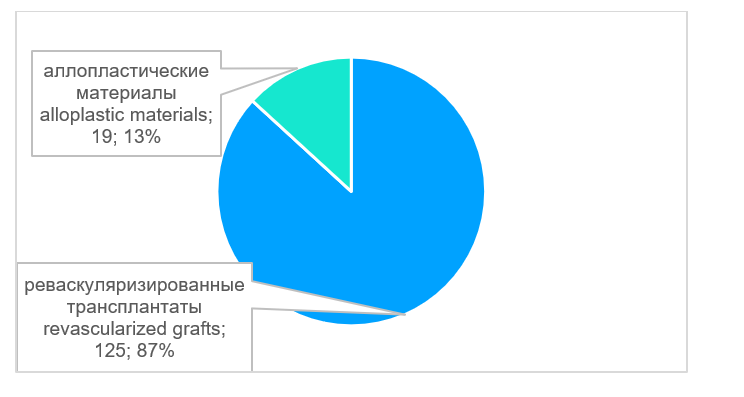
Рис. 6. Примененные пластические материалы, n = 144
Fig. 6. Applied plastic materials, n = 144
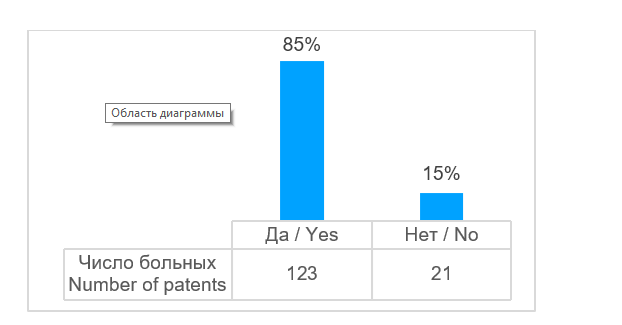
Рис. 7. Применение аддитивных технологий, n = 144
Fig. 7. Applied additive technologies, n = 144
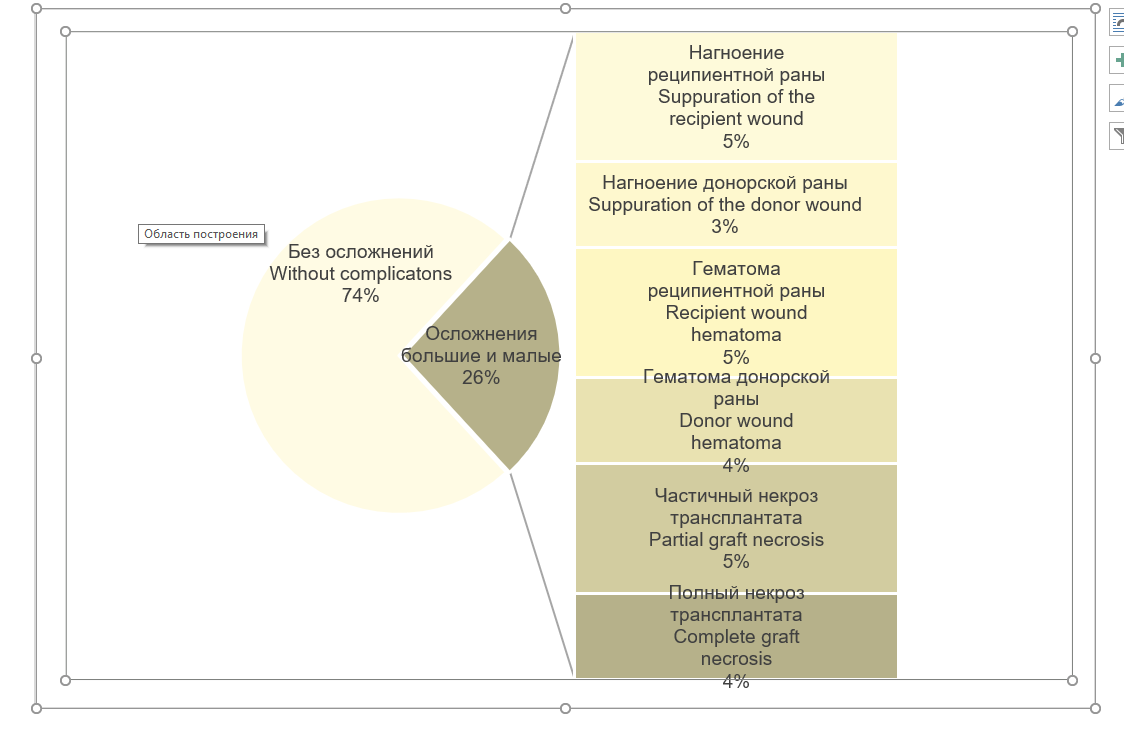
Рис. 8. Послеоперационные осложнения у больных после оперативных вмешательств по устранению дефектов костей лицевого скелета и свода черепа с использованием шаблонов
Fig. 8. Postoperative complications in patients with facial skeleton and cranial vault bones defects
undergone the use of surgical templates during reconstructive operations
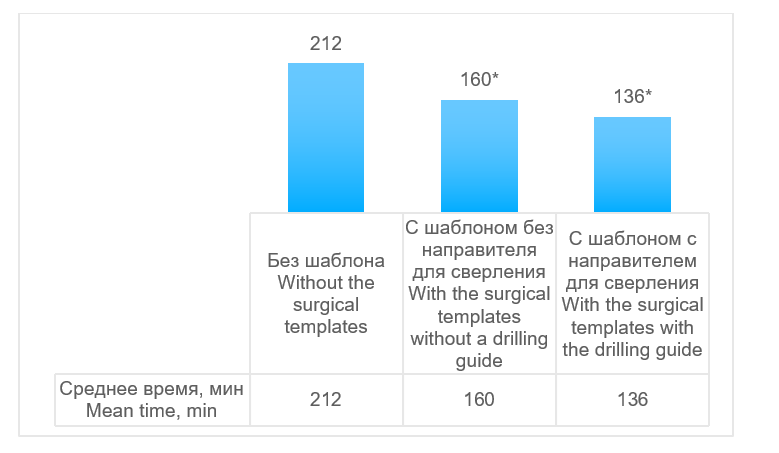
* p <0,001
Рис. 9. Сравнение времени на забор и формирование малоберцового трансплантата при различных методиках выполнения операции
Fig. 9. Comparison of operative time for peroneal graft fence and formation by the surgical technology
[1] Хирулен - так называемый сверхвысокомолекулярный полиэтилен UHMWPE (Ultra High Molecular Weight Polyethylene), обладающий высокой износостойкостью; синонимы: полиэтилен с высоким модулем упругости (англ. High modulus polyethylene, HM PE) и полиэтилен с высокими эксплуатационными характеристиками (англ. High performance polyethylene, HP PE) (прим. авт.).
1. Joskowicz L., Taylor R.H. Computers in imaging and guided surgery // Comput. Sci. Eng. 2001. Vol. 3, № 5. P. 65-72. DOI: https://doi.org/10.1109/5992.947109.
2. Hanasono M.M., Skoracki R.J. Computer-assisted design and rapid prototype modeling in microvascular mandible reconstruction // Laryngoscope. 2013. Vol. 123, № 3. P. 597-604. DOI: https://doi.org/10.1002/lary.23717.
3. Toto J.M. et al. Improved operative efficiency of free fibula flap mandible reconstruction with patient-specific, computer-guided preoperative planning // Head Neck. 2015. Vol. 37, № 11. P. 1660-1664. DOI: https://doi.org/10.1002/hed.23815.
4. Wilde F. et al. Mandible reconstruction with patient-specific pre-bent reconstruction plates: comparison of a transfer key method to the standard method-results of an in vitro study // Int. J. Comput. Assist. Radiol. Surg. 2012. Vol. 7, № 1. P. 57-63. DOI: https://doi.org/10.1007/s11548-011-0599-8.
5. Wang J.C., Nagy L., Demke J.C. Image-guided surgery and craniofacial applications: mastering the unseen // Maxillofac. Plast. Reconstr. Surg. 2015. Vol. 37, № 1. P. 43. DOI: https://doi.org/10.1186/s40902-015-0037-x.
6. ISO / ASTM52900-15, Standard Terminology for Additive Manufacturing - General Principles - Terminology [Электронный ресурс] // ASTM International: [сайт]. URL: http://www.astm.org/cgi-bin/resolver.cgi?ISOASTM52900 (дата обращения 10.04.2019).
7. Жук Д.М., Перфильев С.А. CAS системы - системы автоматизированного проектирования в хирургии // Наука и образование: сетевой журн. 2011. URL: http://technomag.edu.ru/doc/168885.html (дата обращения: 10.05.2019).
8. Rodby K.A. et al. Advances in oncologic head and neck reconstruction: Systematic review and future considerations of virtual surgical planning and computer aided design/computer aided modeling // J. Plast. Reconstr. Aesthetic Surg. 2014. Vol. 67, № 9. P. 1171-1185. DOI: https://doi.org/10.1016/j.bjps.2014.04.038.
9. Burkey B.B., Coleman J.R. Current concepts in oromandibular reconstruction. // Otolaryngol. Clin. North Am. 1997. Vol. 30, № 4. P. 607-630.
10. Hidalgo D.A., Pusic A.L. Free-Flap Mandibular Reconstruction: A 10-Year Follow-Up Study // Plast. Reconstr. Surg. 2002. Vol. 110, № 2. P. 438-449. DOI: https://doi.org/10.1097/00006534-200208000-00010.
11. Robb G. Free-Flap Mandibular Reconstruction: A 10-Year Follow-up Study // Arch. Facial Plast. Surg. 2004. Vol. 6, № 1. P. 65. DOI: https://doi.org/10.1001/archfaci.6.1.65.
12. Prisman E. et al. Value of preoperative mandibular plating in reconstruction of the mandible // Head Neck. 2014. Vol. 36, № 6. P. 828-833. DOI: https://doi.org/10.1002/hed.23382.
13. Haddock N.T. et al. Increasing Bony Contact and Overlap With Computer-Designed Offset Cuts in Free Fibula Mandible Reconstruction // J. Craniofac. Surg. 2012. Vol. 23, № 6. P. 1592-1595. DOI: https://doi.org/10.1097/SCS.0b013e318257576c.
14. Wong A.K. et al. Analysis of risk factors associated with microvascular free flap failure using a multi-institutional database // Microsurgery. 2015. Vol. 35, № 1. P. 6-12. DOI: https://doi.org/10.1002/micr.22223.
15. Sharaf B. et al. Importance of Computer-Aided Design and Manufacturing Technology in the Multidisciplinary Approach to Head and Neck Reconstruction // J. Craniofac. Surg. 2010. Vol. 21, № 4. P. 1277-1280. DOI: https://doi.org/10.1097/SCS.0b013e3181e1b5d8.
 Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International
Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International