Москва, г. Москва и Московская область, Россия
Россия
Россия
Россия
Россия
АНО ДПО "Московский медико-социальный институт имени Ф.П. Гааза" (Кафедра профилактической медицины медицинского факультета, Заведующий кафедрой)
Москва, Россия
ВАК 14.01.2026 Сердечно-сосудистая хирургия
УДК 61 Медицина. Охрана здоровья
ГРНТИ 76.29 Клиническая медицина
BISAC MED010000 Cardiology
BISAC MED032000 Geriatrics
BISAC MED085050 Surgery / Vascular
Введение. Стеноз аортального клапана является самой частой клапанной патологией у кардиохирургических пациентов: операции коррекции стеноза аортального клапана составляют от 10 до 22 % оперативных вмешательств, выполняемых на открытом сердце. 30% больным старческого возраста ввиду тяжелой сопутствующей патологии и высокой предполагаемой операционной летальностью отказывают в протезировании аортального клапана в условиях искусственного кровообращения. С появлением возможности использования малоинвазивных методов лечения, как внутриаортальная баллонная вальвулопластика аортального клапана и транскатетерная имплантация аортального клапана, возникла проблема выбора метода хирургической коррекции выраженного аортального стеноза для данной группы. Целью исследования был выбор метода хирургической коррекции выраженного аортального стеноза у больных старческого возраста, определение места внутриаортальной вальвулопластики в лечении и создание алгоритма оказания медицинской помощи больным этой группы. Пациенты и методы. В исследование были включены 122 больных старше 75 лет с выраженным аортальным стенозом, подтвержденным при эхокардиографии (площадь аортального отверстия менее 1 см2, средний градиент давления на аортальном клапане более 40 мм рт. ст., скорость кровотока более 4,0 м/с), проходящие лечение в центре сердечно-сосудистой хирургии Главного военного клинического госпиталя им. академика Н. Н. Бурденко в 2010 – 2017 гг. Больным первой группы (n = 89) из-за высокого хирургического риска проводилась только консервативная медикаментозная терапия, больным второй группы (n = 12) проведено протезирование аортального клапана в условиях искусственного кровообращения, больным третье группы (n = 8) была выполнена баллонная вальвулопластика аортального клапана, после чего 7 из них вошли в четвертую группу, больным четвертой группы (n = 20) была выполнена ТИАК. Результаты. В максимальный срок наблюдения (3 года) летальность больных первой группы составила 49,5 %, выраженность хронической сердечной недостаточности (ХСН) у большей части выживших больных была на уровне III - IV функционального класса по NYHA; летальность во второй группе наблюдения составила 16,6 %, отмечено уменьшение выраженности ХСН - переход большинства пациентов из III - IV во II функциональный класс ХСН по NYHA; у 7 из 8 больных третьей группы после выполнения вальвулопластики аортального клапана отмечена стабилизация гемодинамики - у 5-ти больных отмечено снижение проявлений ХСН до III ФК и у 2 больных - до II ФК по NYHA, все они вошли в четвертую группу, в которой после выполнения ТИАК за время трехлетнего наблюдения летальности не отмечено. Выводы. У больных старческого возраста хирургическое лечение выраженного аортального стеноза является методом выбора и позволяет достоверно увеличить годичную и трёхлетнюю выживаемость. В группе пациентов старческого возраста с высоким хирургическим риском эндоваскулярная коррекция аортального стеноза является предпочтительной. Баллонная вальвулопластика аортального клапана может быть рассмотрена как этап хирургического лечения выраженного аортального стеноза у больных крайне высокого хирургического риска. Следующим этапом у данной группы больных должны выполняться транскатетерная имплантация аортального клапана. Разработанный алгоритм дифференцированного подхода к выбору метода лечения выраженного аортального стеноза у больных старческого возраста позволяет на 32 % (p <0,05) повысить количество случаев оказания радикальной хирургической помощи больным старческой возрастной группы, ранее считавшимися бесперспективными ввиду невозможности проведения оперативного хирургического лечения.
аортальныйстеноз, транскатетерная имплантация аортального клапана, внутриаортальная баллонная вальвулопластика аортального клапана, старческий возраст
BAV - Balloon aortic valvuloplasty - внутриаортальная баллонная вальвулопластика аортального клапана
BMI - Body Mass Index – индекс массы тела
EuroSCORE - European system for cardiac operative risk evaluation
CIRS-G - Cumulative lllness Rating Scale for Geriatrics - гериатрический кумулятивный индекс коморбидности
DVI - Doppler Velocity Index (the ratio of velocity proximal to the valve, to the velocity through the valve) – скоростной интеграл
NYHA - New York Heart Association - Нью-Йоркская кардиологическая ассоциация
TAVI - Transcatheter Aortic Valve Implantation - транскатетерная имплантация аортального клапана
VTI [of the jet] - Velocity Time Integral [through the prosthesis determined by CW Doppler] – временной интеграл скорости
АК – аортальный клапан
АС – аортальный стеноз
ВАБВП - внутриаортальная баллонная вальвулопластика аортального клапана
ИК – искусственное кровообращение
ИМТ – индекс массы тела
ОРЛ – острая ревматическая лихорадка
ТИАК – транскатетерная имплантация аортального клапана
ФК – функциональный класс
ХСН – хроническая сердечная недостаточность
ЭКС - электрокардиостимуляции
Эхо-КГ – эхокардиография
Введение
Сердечно-сосудистые заболевания занимают первое место среди причин смертности взрослого населения в мире [1]. Патология клапанов сердца – одна из самых частых причин оказания хирургической помощи больным с сердечно-сосудистыми заболеваниями [2]. Самым распространенным приобретенным пороком сердца является аортальный стеноз (АС) [3]. Его этиология неразрывно связана с уровнем развития медицины. До внедрения антибактериальной терапии в широкую практику на первом месте среди причин АС была острая ревматическая лихорадка (ОРЛ) [4]. Снижение заболеваемости ОРЛ во второй половине XX века закономерно привело к тому, что к 1990 г. среди причин АС на первый план уверенно вышел дегенеративный стеноз двустворчатого и трехстворчатого аортального клапана. С начала ХХ1 века самой частой причиной стеноза устья аорты является сенильная дегенерация трехстворчатого аортального клапана (АК).
К сожалению, к настоящему времени не удалось найти терапевтические способы предотвращения развития дегенерации аортального клапана и последующей декомпенсации сердечной деятельности. На сегодняшний день единственным эффективным методом коррекции выраженного стеноза аортального клапана является протезирование аортального клапана [5,6].
Летальность в группе больных старческого возраста, которым было выполнено протезирование аортального клапана, сохраняется на высоком уровне и достигает 15 % [7]. 30% больным ввиду тяжелой сопутствующей патологии и высокой предполагаемой операционной летальностью отказывают в протезировании аортального клапана в условиях искусственного кровообращения [8,9]. Поиск альтернативных методов протезирования аортального клапана на открытом сердце привел к разработке метода внутриаортальной баллонной вальвулопластики [7]. Однако, этот метод оперативного хирургического лечения обеспечивает лишь кратковременную эффективность [10,11], и через 1 - 1,5 месяца наступает рестеноз аортального клапана [12]. Следующим этапом развития малоинвазивной хирургии аортального клапана было создание протеза-стента с разработкой и внедрением технологии транскатетерной импланации аортального клапана ТИАК [13–15]
Целью исследования был выбор метода хирургической коррекции выраженного АС у больных старческого возраста, определение места внутриаортальной вальвулопластики в лечении и создание алгоритма оказания медицинской помощи больным этой группы.
Материалы и методы
В центре сердечно-сосудистой хирургии ГВКГ им. академика Н.Н. Бурденко в 2010 - 2017 гг. проходило лечение 643 больных с аортальным стенозом, диагностика и лечение проводились по рекомендациям Рабочей группы по ведению пациентов с клапанной болезнью сердца Европейского общества кардиологов (The European Society of Cardiology - ESC) и Европейской ассоциации кардио-торакальной хирургии (The European Association for Cardio-Thoracic Surgery - EACTS) [16,17]. Критериями включения в исследование были: наличие выраженного аортального стеноза, подтвержденного при эхокардиографии (площадь аортального отверстия менее 1 см2, средний градиент давления на АК более 40 мм рт. ст., скорость кровотока более 4,0 м/с) и возраст больных более 75 лет. Из 643 пациентов были отобраны 122 пациента, соответствующих вышеуказанным критериям включения. Клиническая характеристика больных представлена в таблицах 1, 2, 3.
Таблица 1. Пол, возраст, индекс массы тела больных (n = 122)
Table 1. Sex, Age and BMI of patients (n = 122)
|
Параметры |
n |
% |
|
Число пациентов, всего Patients, in total |
122 |
100 % |
|
Мужчин Man |
100 |
82 % |
|
Женщин Femail |
22 |
18 % |
|
Средний возраст, лет Age, years old, Mean |
81,7 ± 2,7 |
|
|
Средний индекс массы тела BMI, Mean |
25 ± 2,4 |
|
Таблица 2. Выраженность ХСН у больных при включении в исследование, ФК по NYHA (n = 122)
Table 2. Heart failure in patients, NYHA Class (n = 122)
|
ФК по NYHA NYHA Class |
Число больных, n |
% |
|
II |
29 |
24 % |
|
III |
73 |
60 % |
|
IV |
20 |
16 % |
Таблица 3. Результаты Эхо-КГ у больных при включении в исследование (n = 122)
Table 3. Echocardiographic parameters in patients (n = 122)
|
Показатель Parameter |
Результат Value |
|
Конечно-диастолический размер левого желудочка, см End-diastole Left Ventricular cavity size, cm |
5,5 ± 0,5 |
|
Конечно-систолический размер левого желудочка, см End-systole Left Ventricular cavity size, cm |
3,6 ± 0,7 |
|
Фракция выброса, % Ejection Fraction, % |
60,3 ± 10,3 |
|
Площадь отверстия аортального клапана, см2 Aortic valve area, cm2 |
0,8 ± 0,2 |
|
Средний градиент систолического давления на аортальном клапане, мм рт. ст. Mean pressure gradient (Aortic valve), mmHg |
53,4 ± 13,3 |
|
Максимальная скорость стенотической струи на аортальном клапане, м/с Peak velocity (Aortic valve), m/s |
5,1 ± 0,6 |
|
Скоростной интеграл DVI |
0,18 ±0,03 |
|
Временной интеграл скорости VTI |
0,19 ± 0,02 |
|
Систолическое давление в легочной артерии, мм рт. ст. Pulmonary artery systolic pressure, mmHg |
36,7 ± 11,6 |
Распределение больных по группам исследования представлено на рис. 1. 89 больным ввиду высокого хирургического риска была проведена консервативная терапия. 12 больным предложено протезирование АК в условиях искусственного кровообращения (ИК). 8 больным в связи с тяжестью состояния и декомпенсацией сердечной недостаточности первым этапом выполнена внутриаортальная баллонная вальвулопластика, затем 7 из них выполнена ТИАК. Группа больных, которым выполнена ТИАК, составила 20 человек. Исследование проводилось в соответствии с принципами Хельсинской Декларации девятого пересмотра [1].
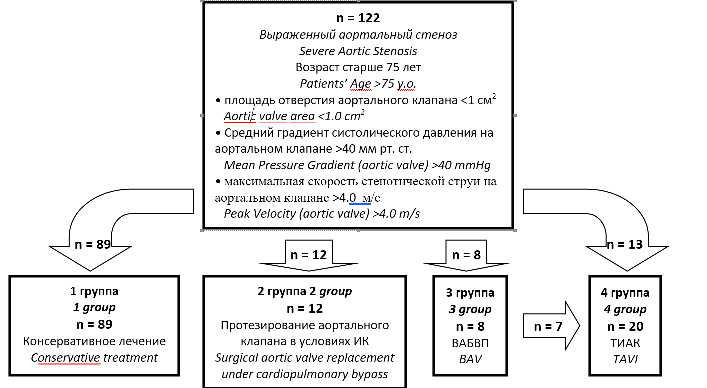
Рис. 1. Распределение больных по группам исследования
Fig. 1. Patients’ groups
Результаты
В первой группе больных (89 человек), которым проводилась медикаментозная терапия в соответствии с национальными клиническими рекомендациями по диагностике и лечению хронической сердечной недостаточности третьего (2009), четвертого (2012), пятого (2016-2017) пересмотров [18–21], отмечена 2 % госпитальная летальность (2 больных), 15,7 % больных (14 человек) погибли в первые 6 месяцев. В максимальный срок наблюдения (3 года) выживаемость этой группы составила 50,5 %, при этом большая часть выживших находилась в III-IV функциональном классе ХСН по NYHA).
Во второй группе больным (12 человек) было выполнено протезирование аортального клапана в условиях искусственного кровообращения. 17 % больных имели IV ФК ХСН по NYHA, 67 % - III ФК, 17 %- II ФК. EuroSCORE I (European system for cardiac operative risk evaluation) [22] составил 22,2 ± 1,6 %, EuroSCORE II [23] - 6,0 ± 0,5 %. Индекс коморбидности Чарльсона (Charlson M.E., в модификации R.A. Deyo) [24] составил 10 ± 2 балла, гериатрический кумулятивный индекс коморбидности CIRS-G (Cumulative lllness Rating Scale for Geriatrics) [25] составил 19 ± 2. Интраоперационной и годичной летальности не отмечено. В раннем послеоперационном периоде инфарктов, инсультов не было. У 40 % больных наблюдалось транзиторное (до 7 суток) нарушение ритма, что потребовало проведение временной электрокардиостимуляции (ЭКС). Всем больным были имплантированы биологические протезы клапанов, время ИК составило 121 ± 30,3 мин, время пережатия аорты - 79,3 ± 15,2 мин. Летальность за 3 года послеоперационного наблюдения составила 16,6 %. Отмечен переход большинства пациентов из III - IV во II функциональный класс ХСН по NYHA.
Больным третьей группы (8 человек) была выполнена баллонная вальвулопластика аортального клапана. Выраженность ХСН у больных (n = 8), которым была выполнена баллонная вальвулопластика аортального клапана, до операции определялась на уровне IV ФК ХСН по NYHA. Средний возраст пациентов составил 84,6 ± 3,25 года. Индекс коморбидности Чарльсона составил 18 ± 5,4 балла, гериатрический кумулятивный индекс коморбидности составил 28 ± 3. Риск по EuroSCORE I составил 69,5 ± 12 %, по EuroSCORE II - 42,3±4 %. Всем больным в предоперационном периоде требовалась инотропная поддержка дофамином (7,6 ± 2,2 мкг/кг/мин). После проведения операции отмечена стабилизация гемодинамики, в связи чем была завершена инотропная поддержка, у 5-ти больных отмечено снижение проявлений ХСН до III ФК и у 2 больных - до IIФК по NYHA (таблица 4). Результаты изменения внутрисердечной гемодинамики представлены в таблице 4. 7 больным следующим этапом была выполнена ТИАК. 2 больным процедура баллонной вальвулопластики выполнялась дважды, так как на момент операции были абсолютные противопоказаний к радикальной коррекции порока аортального клапана. Один больной, 88 лет, с крайне высоким индексом коморбидности Чарльсона (вероятность погибнуть в течение года - 94%, в данную госпитализацию - 50%) погиб от прогрессирования сердечной недостаточности на 4 день после второй процедуры ВАБВП. При патологоанатомическом исследовании макроскопических признаков разрыва створок выявлено не было, что можно объяснить разъединением створок аортального клапана методом баллонной вальвулопластики по ходу комиссур. Диаметр отверстия аортального клапана составил 13 мм, что является доказательством эффективной вальвулотомии аортального клапана внутриаортальным баллоном.
Таблица 4. Выраженность ХСН у больных до и после операции ВАБВП, ФК по NYHA (n = 8)
Table 4. Patients’ NYHA Class before and after BAV (n = 8)
|
ФК по NYHA NYHA Class
|
До операции ВАБВП Before BAV |
После операции ВАБВП After BAV |
||
|
Число больных Patients, n |
% |
Число больных Patients, n |
% |
|
|
II |
- |
- |
2 |
25 % |
|
III |
- |
- |
5 |
62,5 % |
|
IV |
8 |
100 % |
1 |
12,5 % |
Таблица 5. Результаты ЭхоКГ у больных до и после операции ВАБВП (n=8)
Table 5. Echocardiographic parameters before and after BAV (n = 8)
|
Показатель Parameter |
До операции БАБВП Before BAV |
1-е сутки после ВАБВП 1st day after BAV |
|
Максимальный градиент систолического давления на аортальном клапане, мм рт. ст. Max pressure gradient (Aortic valve), mmHg |
108 ± 15 |
88,3 ±12,6 |
|
Средний градиент систолического давления на аортальном клапане, мм рт. ст. Mean Pressure gradient (Aortic Valve), mmHg |
50 ± 12 |
43,3 ± 7,5 |
|
Максимальная скорость стенотической струи на аортальном клапане, м/с Peak velocity (Aortic Valve), m/s |
5,0 ± 0,3 |
4,05 ± 0,3 |
|
Скоростной интеграл DVI |
0,18 ± 0,01 |
0,22 ± 0,04 |
|
Временной интеграл скорости VTI |
0,19 ± 0,02 |
0,26 ± 0,03 |
20 больным четвертой группы было выполнено ТИАК. Риск по EuroSCORE I составил 46,4 ± 5,3 %, EuroSCORE II - 5,0 ± 0,8%. Индекс коморбидности Чарльсона составил 23 ± 2 балла, гериатрический кумулятивный индекс коморбидности - 25 ± 2. Продолжительность операции составила 84 ± 11 мин. Время рентгеноскопии - 12 мин. Среднее количество йодсодержащего контраста, потребовавшегося для выполнения процедуры - 300 мл.
Всем больным, перенесшим ТИАК и протезирование аортального клапана в условиях искусственного кровообращения (n = 39) был имплантирован клапан CORE Valve Transcatheter Aortic Valve (Medtronic, США) 23-31 размеров. Четырем больным потребовалась установка постоянной системы ЭКС. В максимальный срок послеоперационного наблюдения (3 года) летальности не отмечено.
Продолжительность пребывания в отделении реанимации и в стационаре была меньше у больных, которым была выполнена ТИАК, в сравнении с больными после протезирования АК с ИК (2,3 ± 1,4 суток против 3,6 ± 1,2 суток и 4,6 ± 1,7 суток против 12,8 ± 3,7 суток соответственно (p <0,05)). Выраженность ХСН у всех пациентов после операции протезирования аортального клапана соответствовала II ФК по NYHA.
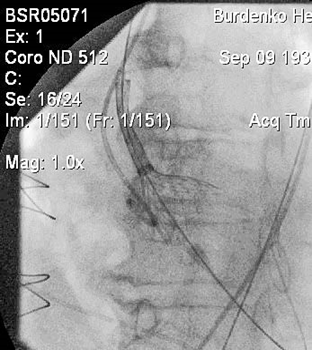
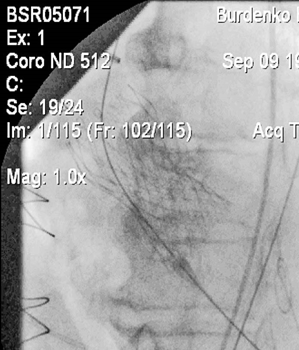
Рис. 2. Транскатетерная имплантация аортального клапана
Пациент Д., 78 лет. Диагноз: Выраженный дегенеративный аортальный стеноз. ХСН 2B, IV ФК. Аортокоронарное шунтирование в анамнезе.
Fig. 2. Transcatheter Aortic Valve Implantation
Patient D., 78 years old. Diagnosis: Severe degenerative aortic stenosis. Heart Failure, Functional Capacity II, Objective Assessment B. A history of coronary artery bypass grafting.
Обсуждение
В 2010 - 2013 гг. в нашей клинике пролечено 60 больных с выраженным аортальным стенозом старше 75 лет. Все больные были обследованы и осмотрены мультидисциплинарным консилиумом для выявления и коррекции сопутствующей патологии. До 2013 г. применялось два варианта лечения таких больных: консервативная терапия и операция протезирования аортального клапана в условиях искусственного кровообращения. Более чем в 50% случаях возможность радикальной коррекции порока была сопряжена с крайне высоким риском для пациента, определяемым по шкалам EuroSCORE I и EuroSCORE II. Доминирующие позиции среди причин, по которым больным не была выполнена хирургическая коррекция порока аортального клапана, занимали рецидивирующее течение онкологического процесса (25 %) и отказ больного от лечения (25 %) (рис. 3).
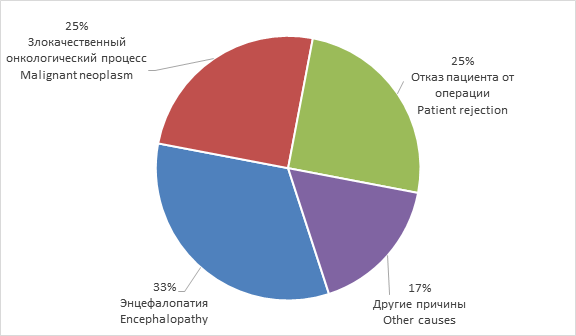
Рис. 3. Причины отказа в хирургическом лечении выраженного аортального стеноза у больных старше 75 лет (n = 60)
Fig. 3. Reasons for rejection in surgical treatment of severe aortic stenosis in senile patients (n = 60)
У 33 % больных были абсолютные противопоказания к операции: болезни крови, тяжелая хроническая обструктивная болезнь легких, острая фаза системной болезни (ревматоидный артрит, миеломная болезнь), обострение язвенной болезни желудка. Из 60 пациентов, которые имели показания к протезированию АК, лишь 10 % было проведено радикальное лечение болезни.
С 2013 г. в центре сердечно-сосудистой хирургии ГВКГ Н.Н. Бурденко внедрены методики эндоваскулярной коррекции аортального стеноза: внутриаортальная баллонная вальвулопластика аортального клапана и транскатетерная имплантация аортального клапана. Появление новых методов лечения продиктовало модернизацию применяемого ранее в госпитале алгоритма лечения выраженного аортального стеноза, по которому все больные подлежали либо хирургическому лечению в объеме протезирования аортального клапана механическим или биологическим протезом в условиях искусственного кровообращения, либо, при непереносимости последнего, консервативной терапии.
В 2013 г. в центре сердечно-сосудистой хирургии ГВКГ Н.Н. Бурденко был разработан новый алгоритм лечения таких пациентов (рис. 4). Отдельным (подготовительным) методом лечения больных с выраженным аортальным стенозом становится внутриаортальная баллонная вальвулопластика. В связи с кратковременность эффекта ВАБВП, требуются дополнительные процедуры ВАБВП или протезирование АК на следующих этапах хирургического лечения. Мы рассматриваем ВАБВП как этап хирургического лечения больных с выраженным АС, имеющих абсолютные противопоказания к радикальной коррекции порока сердца (как к протезированию аортального клапана в условиях искусственного кровообращения, так и ТИАК). Следующим этапом у данной группы больных должна выполняться ТИАК.
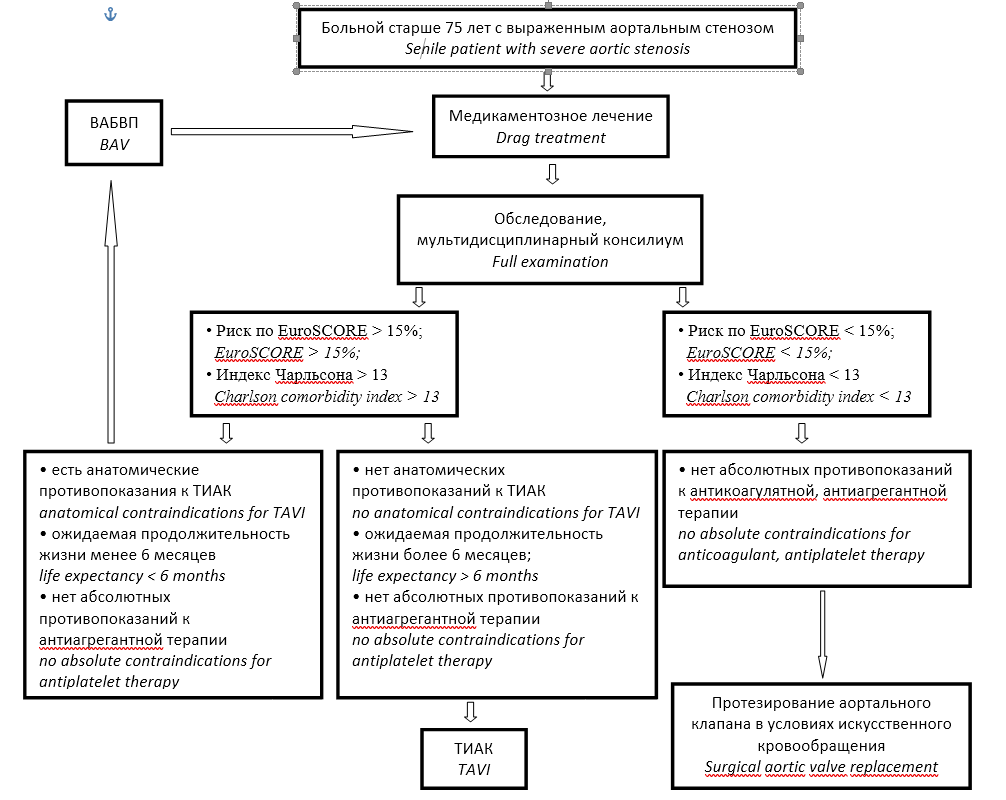
Рис. 4. Алгоритм выбора метода лечения выраженного аортального стеноза у больных cтарческого возраста высокого хирургического риска
Fig. 4. The algorithm for choosing a treatment method of severe aortic stenosis in senile patients with high surgical risk
Использование этого алгоритма позволило более чем на 30% повысить количество случаев оказания радикальной коррекции порока аортального клапана у больных из ранее считавшейся бесперспективной группы возрастных больных. Результаты эффективности использования алгоритма приведены в таблице 6.
Таблица 6. Результаты применения алгоритма лечения выраженного аортального стеноза у больных старше 75 лет (n = 60)
Table 6. The results of using algorithm for severe aortic stenosis treatment in senile patients (n = 60)
|
|
До внедрения алгоритма Before algorithm implementation |
После внедрения алгоритма After algorithm implementation |
|
Количество больных с выраженным АС старше 75 лет Senile patients with severe aortic stenosis, n |
60 |
65 |
|
Количество протезирования АК с ИК Prosthetic aortic valve in patients in conditions of assisted circulation, n |
6 |
7 |
|
Количество процедур ВАБП Balloon aortic valvuloplasty (BAV) in patients, n |
0 |
10 |
|
Количество ТИАК Transcatheter Aortic Valve Implantation (TAVI) in patients, n |
0 |
20 |
|
Доля больных, которым была выполнена радикальная коррекция АС, % Patients who underwent radical correction, % |
10 % |
41,53 % |
- В группе пациентов старческого возраста (старше 75 лет) с высоким хирургическим риском эндоваскулярная коррекция аортального стеноза является предпочтительной.
- Баллонная вальвулопластика аортального клапана может быть рассмотрена как этап хирургического лечения выраженного аортального стеноза у больных крайне высокого хирургического риска. Следующим этапом у данной группы больных должны выполняться ТИАК.
- У больных старческого возраста хирургическое лечение выраженного аортального стеноза является методом выбора и позволяет достоверно увеличить годичную и трёхлетнюю выживаемость. Разработанный алгоритм дифференцированного подхода к выбору метода лечения выраженного аортального стеноза у больных старческого возраста позволяет на 32 % (p <0,05) повысить количество случаев оказания радикальной хирургической помощи больным старческой возрастной группы, ранее считавшимися бесперспективными ввиду невозможности проведения оперативного хирургического лечения.
[1] Хельсинкская декларация (DeclarationofHelsinki) - набор этических принципов для медицинского сообщества, касающихся исследовательской этики и экспериментов на людях; разработана Всемирной медицинской ассоциацией (World Medical Association), девятый пересмотр проведен в октябре 2013 (64th WMA General Assembly, Fortaleza, Brazil). Доступ по ссылке https://www.wma.net/policies-post/wma-declaration-of-helsinki-ethical-principles-for-medical-research-involving-human-subjects/
1. Mathers C.D. et al. Global patterns of healthy life expectancy in the year 2002 // BMC Public Health. 2004. Vol. 4, № 1. P. 66. DOI: https://doi.org/10.1186/1471-2458-4-66.
2. Baumgartner H. Aortic stenosis: medical and surgical management // Heart. 2005. Vol. 91, № 11. P. 1483-1488. DOI: https://doi.org/10.1136/hrt.2004.056176.
3. Iung B. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on Valvular Heart Disease // Eur. Heart J. 2003. Vol. 24, № 13. P. 1231-1243. DOI: https://doi.org/10.1016/S0195-668X(03)00201-X.
4. Sadée A.S., Becker A.E., Verheul J.A. The congenital bicuspid aortic valve with post-inflammatory disease-a neglected pathological diagnosis of clinical relevance // Eur. Heart J. 1994. Vol. 15, № 4. P. 503-506. DOI: https://doi.org/10.1093/oxfordjournals.eurheartj.a060534.
5. Brennan J.M. et al. Long-Term Survival After Aortic Valve Replacement Among High-Risk Elderly Patients in the United States // Circulation. 2012. Vol. 126, № 13. P. 1621-1629. DOI: https://doi.org/10.1161/CIRCULATIONAHA.112.091371.
6. Walther T. et al. Contemporary management of aortic stenosis: surgical aortic valve replacement remains the gold standard // Heart. 2012. Vol. 98, № Suppl 4. P. iv23-iv29. DOI: https://doi.org/10.1136/heartjnl-2012-302399.
7. Paul J. et al. Inoperable severe aortic valve stenosis in geriatric patients: treatment options and mortality rates. // J. Geriatr. Cardiol. 2018. Vol. 15, № 11. P. 703-707. DOI: https://doi.org/10.11909/j.issn.1671-5411.2018.11.001.
8. Leon M.B. et al. Transcatheter Aortic-Valve Implantation for Aortic Stenosis in Patients Who Cannot Undergo Surgery // N. Engl. J. Med. 2010. Vol. 363, № 17. P. 1597-1607. DOI: https://doi.org/10.1056/NEJMoa1008232.
9. Bakaeen F.G. et al. Severe Aortic Stenosis in a Veteran Population: Treatment Considerations and Survival // Ann. Thorac. Surg. 2010. Vol. 89, № 2. P. 453-458. DOI: https://doi.org/10.1016/j.athoracsur.2009.10.033.
10. Percutaneous balloon aortic valvuloplasty. Acute and 30-day follow-up results in 674 patients from the NHLBI Balloon Valvuloplasty Registry. // Circulation. 1991. Vol. 84, № 6. P. 2383-2397. DOI: https://doi.org/10.1161/01.CIR.84.6.2383.
11. Wang A., Kevin Harrison J., Bashore T.M. Balloon aortic valvuloplasty // Prog. Cardiovasc. Dis. 1997. Vol. 40, № 1. P. 27-36. DOI: https://doi.org/10.1016/S0033-0620(97)80020-5.
12. Osnabrugge R.L.J. et al. Aortic Stenosis in the Elderly // J. Am. Coll. Cardiol. 2013. Vol. 62, № 11. P. 1002-1012. DOI: https://doi.org/10.1016/j.jacc.2013.05.015.
13. Chitsaz S. et al. Operative Risks and Survival in Veterans With Severe Aortic Stenosis: Surgery Versus Medical Therapy // Ann. Thorac. Surg. 2011. Vol. 92, № 3. P. 866-872. DOI: https://doi.org/10.1016/j.athoracsur.2011.04.028.
14. Kapadia S.R. et al. Long-Term Outcomes of Inoperable Patients With Aortic Stenosis Randomly Assigned to Transcatheter Aortic Valve Replacement or Standard Therapy // Circulation. 2014. Vol. 130, № 17. P. 1483-1492. DOI: https://doi.org/10.1161/CIRCULATIONAHA.114.009834.
15. Крюков Е.В. и др. Первый опыт транскатетерной имплантации аортального клапана в многопрофильном лечебном учреждении // Вестник Национального медико-хирургического центра им. Н.Н. Пирогова. 2017. Vol. 12, № 1. P. 21-24.
16. Vahanian A. et al. Guidelines on the management of valvular heart disease (version 2012) // Eur. J. Cardio-Thoracic Surg. 2012. Vol. 42, № 4. P. S1-S44. DOI: https://doi.org/10.1093/ejcts/ezs455.
17. Baumgartner H. et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease // Eur. Heart J. 2017. Vol. 38, № 36. P. 2739-2791. DOI: https://doi.org/10.1093/eurheartj/ehx391.
18. Мареев В.Ю. и др. Национальные рекомендации ВНОК И ОССН по диагностике и лечению ХСН (третий пересмотр) // Журнал Сердечная недостаточность. 2010. Vol. 11, № 1. P. 3-62.
19. Мареев В.Ю. и др. Национальные рекомендации ОССН, РКО и РНМОТ по диагностике и лечению ХСН (четвертый пересмотр) // Журнал Сердечная Недостаточность. 2013. Vol. 14, № 7. P. 379-472.
20. Мареев В.Ю. и др. Клинические рекомендации. Хроническая сердечная недостаточность (ХСН) // Журнал Сердечная Недостаточность. 2017. Vol. 18, № 1. P. 3-40. DOI: https://doi.org/10.18087/rhfj.2017.1.2346.
21. Мареев В.Ю. и др. Клинические рекомендации ОССН - РКО - РНМОТ Сердечная недостаточность: хроническая (ХСН) и острая декомпенсированная (ОДСН) Диагностика, профилактика и лечение // Кардиология. 2018. Vol. 17, № S6. P. 1-164. DOI: https://doi.org/10.18087/cardio.2475.
22. Nashef S.A.M. et al. European system for cardiac operative risk evaluation (EuroSCORE) // Eur. J. Cardio-Thoracic Surg. 1999. Vol. 16, № 1. P. 9-13. DOI: https://doi.org/10.1016/S1010-7940(99)00134-7.
23. Roques F. The logistic EuroSCORE // Eur. Heart J. 2003. Vol. 24, № 9. P. 882. DOI: https://doi.org/10.1016/S0195-668X(02)00799-6.
24. Charlson M.E. et al. A new method of classifying prognostic comorbidity in longitudinal studies: Development and validation // J. Chronic Dis. 1987. Vol. 40, № 5. P. 373-383. DOI: https://doi.org/10.1016/0021-9681(87)90171-8.
25. Miller M.D. et al. Rating chronic medical illness burden in geropsychiatric practice and research: Application of the Cumulative Illness Rating Scale // Psychiatry Res. 1992. Vol. 41, № 3. P. 237-248. DOI: https://doi.org/10.1016/0165-1781(92)90005-N.
 Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International
Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International